MinistÃĻre de la SantÃĐ et des Services sociaux
Information pour les professionnels de la santÃĐ
Vaccins
DCaT-HB-VPI-Hib, DCaT-VPI-Hib et DCaT-VPI : vaccins contre la diphtÃĐrie, la coqueluche, le tÃĐtanos, l'hÃĐpatite B, la poliomyÃĐlite et HÃĶmophilus influenzÃĶ de type b
Composition
Plusieurs vaccins inactivés contenant les composants contre la diphtérie, la coqueluche, le tétanos, la poliomyélite et Hæmophilus influenzæde type b sont distribués au Canada :
- Quadracel et Pediacel (Sanofi Pasteur);
- InfanrixâIPV et InfanrixâIPV/Hib (GSK);
- Infanrix hexa (GSK), qui contient le composant contre l’hépatite B en plus des 5 composants mentionnés précédemment.
Chaque dose d’InfanrixâIPV contient :
- 25 unités Lf (30 UI) d’anatoxine diphtérique;
- 3 antigènes purifiés de Bordetella pertussis :
- 25 µg d’anatoxine coquelucheuse,
- 25 µg d’hémagglutinine filamenteuse,
- 8 µg de pertactine;
- 10 unités Lf (40 UI) d’anatoxine tétanique adsorbée;
- une suspension concentrée purifiée de poliovirus inactivés :
- 40 unités d’antigène D de poliovirus de type 1 (Mahoney),
- 8 unités d’antigène D de poliovirus de type 2 (MEF1),
- 32 unités d’antigène D de poliovirus de type 3 (Saukett);
Note : Les poliovirus sont cultivés sur des cellules Vero.
- 0,5 mg de sels d’aluminium;
- des traces de formaldéhyde, de Polysorbate 80, de milieu 199 Hanks, de chlorure de potassium, de phosphate disodique, de phosphate monopotassique, de glycine, de sulfate de néomycine et de sulfate de polymyxine B.
Chaque dose d’InfanrixâIPV/Hib reconstitué contient :
- les composants de l’InfanrixâIPV;
- le vaccin Hiberix : 10 µg d’un polysaccharide capsulaire d’Hæmophilus influenzæ de type b, le PRP purifié et lié par covalence à environ 25 µg d’anatoxine tétanique, 12,6 mg de lactose et 4,5 mg de chlorure de sodium.
On obtient l’InfanrixâIPV/Hib en utilisant l’InfanrixâIPV comme diluant pour le vaccin lyophilisé Hiberix (voir Présentation).
Chaque dose d’Infanrix hexa reconstitué contient :
- les composants de l’InfanrixâIPV/Hib;
- 10 µg d’AgHBs;
- 0,7 mg de sels d’aluminium (plutôt que 0,5 mg comme dans le vaccin InfanrixâIPV);
- 0,12 mg de phosphate d’aluminium;
- ≤ 5 % de protéine de levure et des traces de Polysorbate 20.
On obtient l’Infanrix hexa en utilisant le Pediarix comme diluant pour le vaccin lyophilisé HIberix (voir Présentation). Le Pediarix est un vaccin combiné contre la diphtérie, la coqueluche, le tétanos, l’hépatite B et la poliomyélite; ce vaccin est homologué, mais non commercialisé seul au Canada.
Chaque dose de Quadracel contient :
- 15 unités Lf d’anatoxine diphtérique;
- 5 antigènes purifiés de Bordetella pertussis :
- 20 µg d’anatoxine coquelucheuse,
- 20 µg d’hémagglutinine filamenteuse,
- 5 µg d’agglutinogènes frangés (fimbriæ de types 2 et 3),
- 3 µg de pertactine;
- 5 unités Lf d’anatoxine tétanique;
- une suspension concentrée purifiée de poliovirus inactivés :
- 40 unités d’antigène D de poliovirus de type 1 (Mahoney),
- 8 unités d’antigène D de poliovirus de type 2 (MEF1),
- 32 unités d’antigène D de poliovirus de type 3 (Saukett);
Note : Les poliovirus sont cultivés sur des cellules diploïdes humaines MRCâ5.
- 1,5 mg de phosphate d’aluminium;
- 0,6 % v/v de 2âphénoxyéthanol;
- 10 ppm de Polysorbate 80 et des traces d’albumine bovine sérique, de formaldéhyde, de glutaraldéhyde, de polymyxine B et de néomycine.
Chaque dose de Pediacel contient :
- les composants du Quadracel;
Note : Les poliovirus sont cultivés sur des cellules Vero. - le vaccin ActâHIB :
- 10 µg d’un polysaccharide capsulaire d’Hæmophilus influenzæ de type b, le PRP purifié et lié par covalence à 18-30 µg d’anatoxine tétanique;
- des traces de streptomycine.
| Fabricant | DCaT-VPI | DCaT-VPI-Hib | Hib | DCaT-HB-VPI | DCaT-HB-VPI-Hib |
|---|---|---|---|---|---|
| Sanofi Pasteur | Quadracel | Pediacel | ActâHIB | s.o. | s.o. |
| GSK | InfanrixâIPV | InfanrixâIPV/Hib | Hiberix | Pediarix | Infanrix hexa |
Présentation
- Infanrix hexa :
- Seringue unidose de 0,5 ml de vaccin DCaTâHBâVPI (Pediarix) et fiole unidose de vaccin Hib lyophilisé (Hiberix).
- InfanrixâIPV :
- Seringue unidose de 0,5 ml de vaccin DCaTâVPI.
- InfanrixâIPV/Hib :
- Seringue unidose de 0,5 ml de vaccin DCaTâVPI (InfanrixâIPV) et fiole unidose de vaccin Hib lyophilisé (Hiberix).
- Pediacel :
- Fiole unidose de 0,5 ml de vaccin DCaTâVPIâHib.
- Quadracel :
- Fiole unidose de 0,5 ml de vaccin DCaTâVPI.
Les vaccins ont l’aspect d’une solution trouble et blanchâtre.
Indications
Un programme de vaccination contre l’hépatite B des nourrissons nés depuis le 1er avril 2013 est réalisé au Québec.
 |
Vacciner les enfants âgés de 2 à 47 mois (moins de 4 ans). |
L’enfant qui a eu la diphtérie ou le tétanos doit recevoir la primovaccination complète, car ces maladies ne confèrent pas nécessairement l’immunité.
Les personnes qui ont eu un diagnostic de coqueluche peuvent recevoir sans risque le composant acellulaire de la coqueluche, car l’infection ne confère pas d’immunité à long terme.
L’enfant qui a été atteint de poliomyélite doit être vacciné, car il n’existe pas d’immunité croisée entre les 3 types de poliovirus.
L’enfant qui a eu une infection invasive à Hæmophilus influenzæ de type b doit être vacciné, car l’infection ne confère pas nécessairement l’immunité.
Contreâindications
Anaphylaxie suivant l’administration d’une dose antérieure du même vaccin ou d’un autre produit ayant un composant identique.
Précautions
Voir Vaccinologie pratique, Précautions.
Névrite brachiale
Cette manifestation clinique survient très rarement (de 0,5 à 1 personne vaccinée sur 100 000) après l’administration d’un vaccin comprenant le composant tétanique.
Même si l’association entre la névrite brachiale et le composant tétanique est démontrée, il n’est pas contreâindiqué d’administrer des doses subséquentes de vaccin comprenant ce composant, la névrite brachiale étant généralement réversible.
Syndrome de Guillain-Barré
Les études au cours desquelles ont été révisés des cas de SGB chez des adultes et des enfants permettent de conclure que l’association entre le SGB et le composant tétanique, si cette association existe, est exceptionnelle.
La décision de donner des doses additionnelles de vaccin contenant le composant tétanique à des personnes qui ont été atteintes d’un SGB dans les 6 semaines suivant une dose antérieure doit être basée sur l’évaluation des bénéfices de la poursuite de la vaccination et du risque naturel de récurrence d’un SGB. En général, il est justifié de compléter la vaccination.
Interchangeabilité
Idéalement, il faut suivre le calendrier recommandé (voir Administration). Toutefois, on pourrait changer cette séquence selon le produit disponible afin d’éviter de reporter la vaccination.
Manifestations cliniques après la vaccination
Voir Manifestations cliniques, Présentation des manifestations cliniques.
Risque attribuable au vaccin
Même en l'absence d'études comparatives, la névrite brachiale est considérée comme liée au vaccin (voir Précautions).
Manifestations cliniques observées
| Fréquence | Réactions locales | Réactions systémiques |
|---|---|---|
| Dans la majorité des cas (50 % ou plus) |
Douleur |
Agitation et pleurs inhabituels |
| Très souvent (10 à 49 %) |
Érythème |
Fièvre > 38 °C |
| Souvent (1 à 9 %) |
Douleur importante |
Fièvre > 39,5 °C |
| Parfois (1 à 9 sur 1 000) |
Nodule persistant | s.o. |
| Rarement (1 à 9 sur 10 000) |
s.o. |
Convulsions le plus souvent avec de la fièvre |
| Très rarement (1 à 9 sur 100 000) |
Abcès stérile | Œdème de 1 ou des 2 membres inférieurs |
| Moins de 1 sur 1 million | s.o. | Anaphylaxie |
Ne pas confondre une réaction locale importante (douleur de faible intensité et disparition spontanée après 3 ou 4 jours) avec une cellulite infectieuse, qui s'accompagne généralement de fièvre et d’une atteinte de l'état général.
Au cours de la primovaccination, la seule différence possible entre les vaccins est l’incidence augmentée de fièvre de 38 °C ou plus rapportée avec les vaccins de GSK.
Administration
Administrer l’InfanrixâIPV/Hib et l’Infanrix hexa le plus rapidement possible après leur reconstitution ou au plus tard 8 heures après en les conservant entre 2 et 8 °C.
Bien agiter la fiole ou la seringue avant d’administrer le vaccin. Les sels d’aluminium tendent à former un dépôt blanc au fond de la fiole ou dans la seringue.
Administrer le contenu du format unidose par voie IM.
| Le calendrier régulier des nourrissons inclut l’administration d’un vaccin DCaT-HB-VPI-Hib (hexavalent) à l'âge de 2 et 4 mois ainsi que l'administration d’un vaccin DCaT-VPI-Hib (pentavalent) à l'âge de 1 an. | ||
| Vaccin | Âge | Précisions |
|---|---|---|
|
L’utilisation de vaccins combinés chez les enfants peut entraîner l’administration de doses contre Hæmophilus influenzæ de type b ou la poliomyélite non requises pour la protection, mais cela permet de simplifier le calendrier tout en étant sécuritaire. À compter de l’âge de 4 ans, utiliser un vaccin réduit en antigènes de la diphtérie et de la coqueluche (voir Calendriers de vaccination et les vaccins dcaT-VPI et dcaT). |
||
|
DCaTâHBâVPIâHib |
2 mois et 4 mois |
Âge minimal : 6 semaines Intervalle minimal : 4 semaines Administrer 1 dose de vaccin DCaT-VPI-Hib (pentavalent) à l’âge de 6 mois à ces nourrissons en respectant un intervalle de 8 semaines (intervalle minimal de 4 semaines) depuis la dernière dose de vaccin DCaT-HB-VPI-Hib :
|
|
DCaTâVPIâHib |
1 an |
Âge minimal : 1 an Intervalle minimal : 6 mois |
Prophylaxie antitétanique dans le traitement des plaies chez les enfants âgés de moins de 4 ans
L’algorithme suivant décrit la démarche décisionnelle pour la prophylaxie antitétanique dans le traitement des plaies chez les enfants âgés de moins de 4 ans. L’outil interactif Aide à la décision pour la prophylaxie antitétanique ![]() permet d’arriver aux mêmes conduites à tenir. L'enfant considéré comme protégé contre le tétanos (voir Calendriers de vaccination) qui présente une plaie n'a pas besoin de prophylaxie antitétanique, à l’exception de l’enfant immunodéprimé(4).
permet d’arriver aux mêmes conduites à tenir. L'enfant considéré comme protégé contre le tétanos (voir Calendriers de vaccination) qui présente une plaie n'a pas besoin de prophylaxie antitétanique, à l’exception de l’enfant immunodéprimé(4).
Administrer la prophylaxie contre le tétanos le plus tôt possible, de préférence dans les 3 jours suivant la blessure. Administrer la prophylaxie même si ce délai est dépassé, car la période d’incubation du tétanos peut être longue (elle dépasse rarement 3 semaines).
L’âge minimal d’administration du vaccin est de 6 semaines. Il n’y a pas d’âge minimal pour l’administration des TIg.
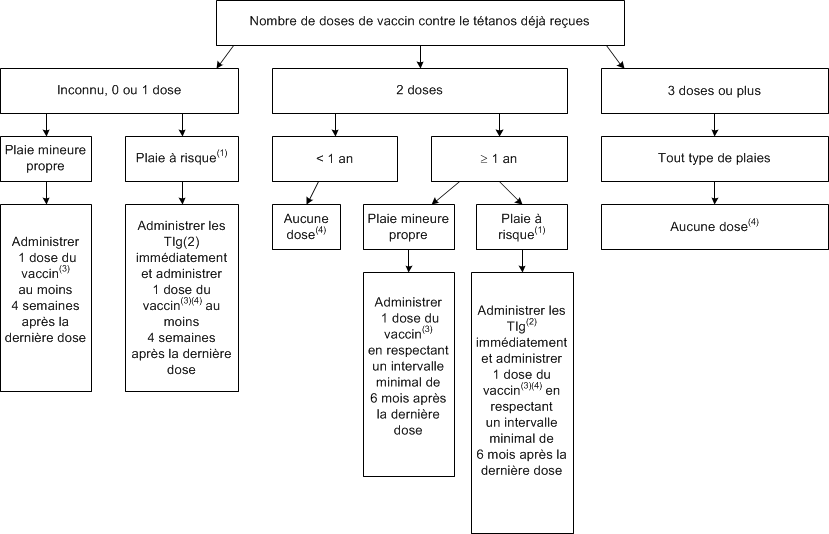
- Plaie à risque d’infection par Clostridium tetani : plaie contaminée par de la poussière, de la salive humaine ou animale, des selles ou de la terre, plaie pénétrante (due, par exemple, à une morsure ou à un clou rouillé), plaie contenant des tissus dévitalisés, plaie nécrotique ou gangreneuse, engelure, brûlure ou avulsion. Le nettoyage et le débridement de la plaie sont indispensables. Les plaies chroniques (ex. : plaie de pression, ulcère des membres inférieurs), les piqûres et morsures d’insectes ainsi que les chirurgies abdominales ne sont pas considérées d’emblée comme des plaies à risque d’infection par Clostridium tetani.
- La posologie des TIg est de 1 ml (250 unités) par voie IM (voir TIg). Le vaccin sera administré à un site différent.
- On administre le vaccin DCaT-VPI-Hib, avec ou sans le composant HB selon les antécédents de vaccination de l’enfant (voir Administration).
- Chez l’enfant immunodéprimé, administrer le vaccin et les TIg en présence d’une plaie à risque, quel que soit l’intervalle depuis la dernière dose de vaccin.
Pour avoir accès à une présentation différente de cette information, voir TIg, Tableau synthèse des produits à administrer pour la prophylaxie du tétanos chez les enfants âgés de moins de 4 ans.
Administrer les TIg même si 1 dose de vaccin a déjà été administrée en postexposition :
- jusqu’à 7 jours après le vaccin si 1 ou 2 doses de vaccin ont été reçues avant la blessure;
- jusqu’à 14 jours après le vaccin si aucune dose de vaccin n’a été reçue avant la blessure.
Si aucun produit n’a été administré, administrer le vaccin et les TIg :
- jusqu’à 7 jours après la blessure si 1 ou 2 doses de vaccin ont été reçues avant la blessure;
- jusqu’à 21 jours après la blessure si aucune dose de vaccin n’a été reçue avant la blessure.
Si ces délais sont dépassés, administrer le vaccin seul pour protéger contre des expositions futures.
Réponse au vaccin
Immunogénicité
Après une série complète de 2 doses suivies de 1 dose de rappel avec le vaccin DCaT-HB-VPI-Hib, près de 98 % des enfants vaccinés obtiennent des titres d’anticorps protecteurs contre tous les antigènes contenus dans le vaccin.
Diphtérie
Un mois après la 2e dose de vaccin, de 99,6 % des enfants vaccinés obtiennent un titre d’anticorps protecteur contre la diphtérie, et la 3e dose permet à 100 % des enfants de dépasser ce titre.
Tétanos
Un mois après la 2e dose de vaccin et un mois après la 3e dose, 100 % des enfants vaccinés dépassent le titre d’anticorps protecteur contre le tétanos.
Coqueluche
Il n’existe pas de consensus sur les titres d’anticorps protecteurs contre la coqueluche. Dans diverses études, la réponse à la vaccination varie de 77 à 100 % pour chacun des antigènes coquelucheux contenus dans le vaccin. La 4e dose amène une réponse anamnestique chez 94â99 % des enfants.
Poliomyélite
Un mois après la 2e dose de vaccin, de 86 à 93 % des enfants vaccinés obtiennent des titres d’anticorps protecteurs contre les 3 types de poliovirus. Un mois après la 3e dose, 98 % des enfants obtiennent ce titre.
Hæmophilus influenzæ de type b
Un mois après la 2e dose de vaccin, 84 % des enfants en bonne santé obtiennent un titre d’anticorps protecteur contre Hæmophilus influenzæ de type b, et la 3e dose permet à 94 % des enfants de dépasser le titre d’anticorps qui indique une protection à long terme. Les données disponibles montrent que l’immunogénicité du calendrier à 2 mois, 4 mois et 1 an de vie chez les grands prématurés (< 32 semaines) et certains enfants immunodéprimés est moins bonne pour certains composants du vaccin DCaT-VPI-Hib (notamment, le composant Hib) après 2 doses administrées avant l’âge de 1 an.
Hépatite B
Un mois après la 2e dose et un mois après la 3e dose de vaccin, au moins 99 % des enfants ont obtenu un titre d’anticorps protecteur contre l’hépatite B.
Efficacité
Diphtérie
Le vaccin protège plus de 95 % des personnes adéquatement vaccinées; toutefois, il n’élimine pas le portage de la bactérie sur la peau ou dans le nasopharynx. La protection dure de nombreuses années après la primovaccination.
Tétanos
La protection conférée par l’anatoxine tétanique est presque de 100 %. La protection dure de nombreuses années après la primovaccination.
Coqueluche
Tous les vaccins acellulaires contre la coqueluche homologués au Canada ont une efficacité d’environ 85 % après 3 doses. L’efficacité est plus importante au cours de la 1re année suivant la vaccination et elle diminue progressivement pendant une période d’environ 10 ans. Généralement, lorsque le vaccin n’empêche pas la maladie, il réduit la gravité des symptômes et la fréquence des complications.
Poliomyélite
Le vaccin protège contre les 3 types de poliovirus près de 100 % des personnes ayant reçu la primovaccination et procure une protection durable, peutâêtre pour la vie.
Hæmophilus influenzæ de type b
Les vaccins DCaT-HB-VPI-Hib et DCaT-VPI-Hib confèrent une protection supérieure à 95 % contre les infections invasives à Hæmophilus influenzæ de type b. Depuis l’introduction des vaccins conjugués au Canada, l’incidence totale de ces infections a chuté de 99 %. Les échecs vaccinaux sont très rares, et la population non vaccinée bénéficie de l’immunité collective induite par la diminution du portage de la bactérie au sein de la population vaccinée. La durée de la protection est inconnue, mais les données actuelles laissent croire qu’elle est de plusieurs années.
Hépatite B
Il n’existe pas de données spécifiques d’efficacité contre l’hépatite B pour le vaccin DCaTâHBâVPIâHib. Toutefois, comme les vaccins combinés donnent le même profil d’immunogénicité, de persistance d’anticorps et de mémoire immunitaire que les composants administrés séparément, il est raisonnable de croire à une efficacité similaire.
Les programmes de vaccination des nourrissons contre l’hépatite B réalisés dans de nombreux pays ont démontré leur efficacité contre l’infection clinique et le portage de l’AgHBs pour une durée de plus de 20 ans. Même si la protection sur de plus longues années est inconnue, la circulation du virus et le risque de contracter l’hépatite B au Québec sont considérablement réduits compte tenu des cohortes de préadolescents vaccinés depuis 1994.
DerniÃĻre mise à jour : 22 juin 2023
