MinistÃĻre de la SantÃĐ et des Services sociaux
Information pour les professionnels de la santÃĐ
Immunologie de la vaccination
ImmunogÃĐnicitÃĐ des vaccins
Plusieurs facteurs peuvent influencer la réponse immunitaire induite par la vaccination. La nature et l’intensité de la réponse varieront en fonction de facteurs liés au vaccin et de facteurs liés à l’hôte.
Facteurs liés au vaccin
Nature de l’antigène
Vaccins vivants atténués
Les particules virales se disséminent rapidement dans l’organisme, se multiplient et activent l’immunité innée puis l’immunité adaptative, comme lors de l’infection naturelle.
Les réactions inflammatoires locales sont rares et sont liées plus au volume injecté qu’à la composition du vaccin.
L’infection est habituellement non apparente. Elle peut être accompagnée de symptômes systémiques atténués (ex. : fièvre, malaises, éruption) après la période nécessaire à la réplication virale (de 7 à 21 jours selon le vaccin).
Le temps nécessaire à l’induction d’anticorps (de 2 à 3 semaines) reflète la durée de différenciation des lymphocytes B dans la rate et les ganglions.
Comparativement aux vaccins inactivés, les vaccins vivants atténués induisent une meilleure réponse immunitaire innée, une production d’anticorps plus importante et plus persistante en raison de la réplication systémique. La conséquence est l’obtention d’un taux d’anticorps plus élevé et plus durable.
Réponse immunitaire humorale provoquée par la rougeole naturelle et par le vaccin contre la rougeole
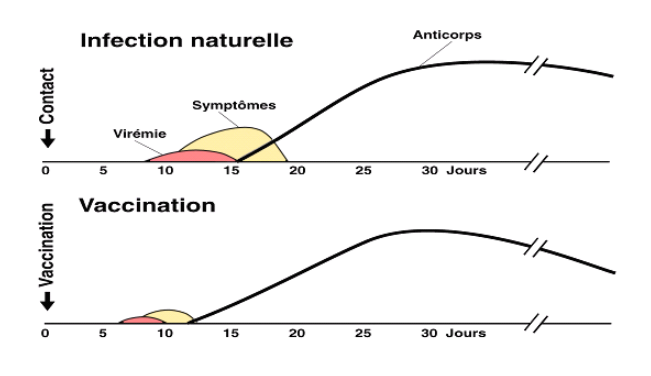
Adapté de Michel REY, Vaccinations
Vaccins inactivés
La réponse immunitaire est variable selon les antigènes des vaccins.
Les Ag vaccinaux sont pris en charge par les cellules dendritiques. Celles-ci provoquent l’activation des cellules inflammatoires et déclenchent la réaction locale. Les cellules dendritiques migrent également vers les ganglions régionaux et peuvent y déclencher de l’inflammation. Cette période dure de 2 à 3 semaines, produisant un pic d’anticorps environ 1 mois après la vaccination.
Les plasmocytes responsables de cette réponse immunitaire primaire meurent rapidement par la suite, entraînant une baisse rapide du taux d’anticorps, d’où la nécessité d’administrer 1 ou plusieurs doses additionnelles, qui entraîneront une réponse anamnestique secondaire.
On distingue plusieurs types de vaccins inactivés :
- Inactivés polysaccharidiques;
- Inactivés polysaccharidiques conjugués à une protéine;
- Inactivés entiers ou inactivés à protéines purifiées;
- Inactivés à ARN messager;
- Inactivés à protéines recombinantes;
- Inactivés à vecteur viral.
|
Type de vaccin |
Caractéristiques |
|---|---|
|
Vaccins entiers ou à protéines purifiées |
Les vaccins inactivés entiers sont constitués de microâorganismes complets, alors que les vaccins inactivés à protéines purifiées contiennent des protéines constituantes des micro-organismes La présence de protéines rend les substances immunogènes et induit une réponse immunitaire humorale (lymphocytes B) et cellulaire (lymphocytes T) Les antigènes sont dits Tâdépendants Ces vaccins sont immunogènes avant l’âge de 2 ans La production de cellules mémoire permet une réponse anamnestique lors d’une nouvelle exposition à ces vaccins |
|
Vaccins polysaccharides conjugués à une protéine |
La conjugaison est le couplage des polysaccharides à une protéine vectrice La réponse immunitaire est apparentée à celle des vaccins inactivés entiers ou inactivés à protéines purifiées et elle possède les mêmes caractéristiques La réponse immunitaire induite est humorale (lymphocytes B) et cellulaire (lymphocytes T) Les principales protéines utilisées pour la conjugaison dans la fabrication des vaccins contre le pneumocoque et le méningocoque sont :
|
|
Vaccins polysaccharidiques |
Les polysaccharides sont des constituants de la membrane externe de la bactérie La réponse immunitaire induite est humorale seulement (lymphocytes B) Les lymphocytes T ne sont pas stimulés Les antigènes sont dits Tâindépendants Ces vaccins sont peu ou pas immunogènes avant l’âge de 2 ans Il n’y a pas de production de cellules mémoire et de réponse anamnestique à la suite d’une nouvelle exposition à ces vaccins |
|
Vaccins à ARN messager |
Un vaccin à ARN messager est constitué de nanoparticules lipidiques contenant de l’ARN messager. Cet ARN messager contient un fragment de l’information génétique du virus Le vaccin à ARN messager est absorbé par les cellules. Dans le cytoplasme de la cellule, il permet de fabriquer une protéine virale qui va stimuler le système immunitaire La réponse immunitaire induite est humorale (lymphocytes B) et cellulaire (lymphocytes T) |
|
Vaccins à protéines recombinantes |
Une protéine recombinante est produite par une cellule (comme une bactérie, une plante, une cellule de mammifère ou encore d’insecte) servant « d’usine vivante » dont le matériel génétique a été modifié avec une séquence de gènes permettant de produire cette protéine ou plusieurs protéines s’assemblant en particules pseudo-virales. Celles-ci sont purifiées et incluses dans le vaccin, qui permettra d’induire une immunité contre le pathogène d’origine de la séquence de gènes |
|
Vaccins à vecteur viral |
Le vecteur viral est un virus inoffensif pour l’humain qui contient le code génétique d’une protéine d’intérêt Une fois absorbé par les cellules, le code génétique permet de fabriquer la protéine qui va stimuler le système immunitaire La réponse immunitaire induite est humorale (lymphocytes B) et cellulaire (lymphocytes T) |
|
Caractéristiques |
Réponse primaire (1er contact avec l’antigène) |
Réponse secondaire (contacts ultérieurs avec l’antigène) |
|---|---|---|
|
Période de latence |
Période relativement longue avant l’apparition des anticorps spécifiques |
Période de latence plus courte avant l’apparition des anticorps spécifiques |
|
Intensité de la réaction |
Intensité faible (habituellement insuffisante pour conférer une protection) |
Intensité plus forte (habituellement suffisante pour conférer une protection) |
|
Avidité des anticorps |
Faible avidité des anticorps |
Forte avidité des anticorps |
|
Durée des anticorps |
Durée courte |
Durée longue |
SCHÉMA DE LA RÉPONSE IMMUNITAIRE INDUITE PAR UN VACCIN INACTIVÉ
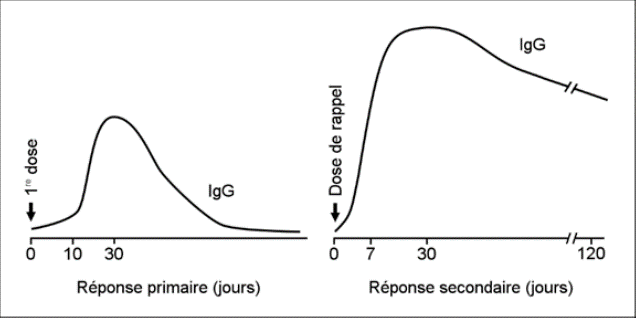
Présence d’un adjuvant
Les adjuvants peuvent être utilisés pour plusieurs raisons :
- Obtenir une meilleure réponse sérologique.
- Renforcer l’immunogénicité du vaccin en favorisant la réaction inflammatoire.
- Assurer une immunité plus durable.
- Utiliser une quantité plus faible d’antigènes.
- Administrer un plus petit nombre de doses.
L’adjuvant le plus fréquemment utilisé est le sel d’aluminium, en général sous forme de phosphate ou d’hydroxyde d’aluminium. Les autres adjuvants utilisés sont :
- Émulsion huile-eau MF59.
- AS01B (Fraction de Quillaja saponaria Molina et 3-O-désacyl-4’— monophosphoryl lipide A).
- Adjuvant AS03 (Polysorbate 80, tocophérol et squalène).
- Adjuvant AS04 (hydroxyde d’aluminium et 3âOâdésacylâ4’— monophosphoryl lipide A).
Voie d’administration
La voie ID est la plus immunogène en raison de la grande quantité de cellules présentatrices d’antigènes (ex. : cellules dendritiques et macrophages) présentes dans le derme.
On observe une faible immunogénicité dans le tissu adipeux, car les cellules dendritiques y sont rares. Ainsi, la faible immunogénicité observée lorsque le vaccin HB est administré dans la fesse est probablement due à l’injection du vaccin dans le tissu adipeux plutôt que dans le muscle.
Posologie
Généralement, lorsque la quantité d’antigènes contenus dans un vaccin est plus élevée, la quantité d’anticorps augmente.
Nombre de doses
La réponse secondaire observée a tendance à augmenter avec le nombre de doses de vaccin administrées si les intervalles minimaux entre les doses de vaccin sont respectés.
Intervalles entre les doses
Une 2e stimulation antigénique trop rapprochée de la 1re peut être inefficace à cause de l’élimination de l’antigène par les anticorps sériques encore présents à une forte concentration, d’où l’importance de respecter les intervalles minimaux entre les doses.
Mécanismes de protection conférée par certains vaccins
Selon leur type, les vaccins peuvent induire des anticorps et des lymphocytes T, qui sont considérés comme des mécanismes essentiels de protection. Ces mécanismes sont présentés dans les tableaux qui suivent.
Il est à noter que les lymphocytes T CD4+ participent à l’induction de toutes les réponses en anticorps, à l’exception de celles qui sont induites par les vaccins polysaccharidiques.
Les tableaux ciâdessous montrent les types de cellules, d'anticorps ou de lymphocytes induits par différents vaccins.
| Vaccins | Mécanismes |
|---|---|
| Poliomyélite (vaccin oral) |
Anticorps neutralisants sériques IgG (++) Anticorps neutralisants muqueux IgG (++) et IgA (++) |
| Rougeole, rubéole, oreillons | Anticorps neutralisants sériques IgG (+++) Lymphocytes T CD8+ (rougeole) |
| Varicelle | Anticorps neutralisants sériques IgG (++) Lymphocytes T CD4+ (+?) |
| Fièvre jaune | Anticorps neutralisants sériques IgG (+++) |
| Tuberculose (BCG) | Lymphocytes T CD4+ (++) |
| Grippe (intranasal) | Anticorps neutralisants sériques IgG (++) Anticorps neutralisants muqueux IgG (+) et IgA (+) Lymphocytes T CD8+ (+) |
| Rotavirus | Anticorps neutralisants sériques IgG (+) Anticorps neutralisants muqueux IgG (+) et IgA (++) |
| Zona | Lymphocytes T CD4+ (++) |
Adapté de J. GAUDELUS, Vaccinologie, p. 2. et de Vaccines, 2018, page 17.
| Vaccins | Mécanismes |
|---|---|
| Coqueluche (vaccin entier) |
Anticorps neutralisants sériques IgG (++) Lymphocytes T CD4+ (+?) |
| Poliomyélite (vaccin inactivé) |
Anticorps neutralisants sériques IgG (++) Anticorps muqueux IgG (+) |
| Hépatite A | Anticorps neutralisants sériques IgG (+++) |
| Rage | Anticorps neutralisants sériques IgG (++) |
Adapté de J. GAUDELUS, Vaccinologie, p. 2. et de Vaccines, 2018, page 17.
| Vaccins | Mécanismes |
|---|---|
| Coqueluche (vaccin acellulaire) |
Anticorps neutralisants sériques IgG (++) Lymphocytes T CD4+ (+?) |
| Grippe (vaccin injectable) |
Anticorps neutralisants sériques IgG (++) Anticorps neutralisants muqueux IgG (+) |
|
Tétanos |
Anticorps neutralisants sériques IgG (+++) |
Adapté de J. GAUDELUS, Vaccinologie, p. 2. et de Vaccines, 2018, page 17.
| Vaccins | Mécanismes |
|---|---|
|
Pneumocoque |
Anticorps neutralisants sériques IgG T-indépendants (++) Anticorps neutralisants muqueux IgG (+) |
Adapté de J. GAUDELUS, Vaccinologie, p. 2. et de Vaccines, 2018, page 17.
| Vaccins | Mécanismes |
|---|---|
|
Hæmophilus influenzæ de type b |
Anticorps neutralisants sériques IgG (+++) Anticorps muqueux IgG (++) |
Adapté de J. GAUDELUS, Vaccinologie, p. 2. et de Vaccines, 2018, page 17.
| Vaccins | Mécanismes |
|---|---|
|
COVID-19 ARNm |
Anticorps neutralisants sériques IgG Lymphocytes T CD4+ (++) et T CD8+ (+) |
| Vaccins | Mécanismes |
|---|---|
|
Hépatite B |
Anticorps neutralisants sériques IgG (++) |
|
VPH |
Anticorps neutralisants sériques IgG anti-VPH |
|
Zona (sous-unitaire) |
Anticorps neutralisants sériques IgG contre la glycoprotéine E du virus varicelleâzona
Génération de lymphocytes T CD4+ contre la glycoprotéine E du virus varicelleâzona |
| Vaccins | Mécanismes |
|---|---|
|
COVID-19 VV |
Anticorps neutralisants sériques IgG |
Facteurs liés à l’hôte
De nombreux facteurs liés à l’hôte peuvent moduler la réponse immunitaire.
Âge au moment de la vaccination
Le système immunitaire du corps humain est fonctionnel dès la naissance et persiste tout au long de la vie. Des différences dans la réponse immunitaire existent selon l’âge, particulièrement chez les très jeunes enfants et les personnes âgées.
Nouveau-nés prématurés
La réponse immunitaire dépend de l’âge après la naissance, et non de l’âge gestationnel. Ainsi, un bébé né à 30 semaines de grossesse recevra ses premiers vaccins quand il atteindra l’âge de 2 mois, même si cet âge correspond à un âge gestationnel de 38 semaines.
Nouveau-nés et nourrissons âgés de moins de 2 ans
La capacité du système immunitaire des enfants âgés de moins de 2 ans est très importante :
- Nombre élevé de lymphocytes naïfs disponibles.
- Capacité de générer jusqu’à 2 millions de lymphocytes T CD4+ chaque jour.
- Capacité de répondre à 10 000 antigènes différents simultanément.
Leur système immunitaire est immature :
- Forte proportion de lymphocytes B et T immatures.
- Centres germinatifs non encore présents dans les tissus lymphoïdes.
- Présence d’une réponse immunitaire aux antigènes Tâdépendants, mais production d’anticorps moindre que chez les enfants plus âgés.
- Absence de réponse immunitaire aux antigènes Tâindépendants, d’où l’absence de réponse ou la faible réponse aux vaccins polysaccharidiques.
Les anticorps de la mère sont présents chez les nouveauânés :
- Ils sont transmis passivement in utero ou par l’allaitement.
- Ils peuvent avoir un effet inhibiteur sur la réponse immunitaire du nourrisson; les calendriers de vaccination en tiennent compte.
- Ils protègent partiellement contre la varicelle, la poliomyélite, la rougeole, les oreillons, la rubéole, la gastroentérite à rotavirus, le tétanos, la diphtérie, la coqueluche et l’infection invasive à Hæmophilus influenzæ de type b.
Schéma de la réponse humorale chez le nourrisson
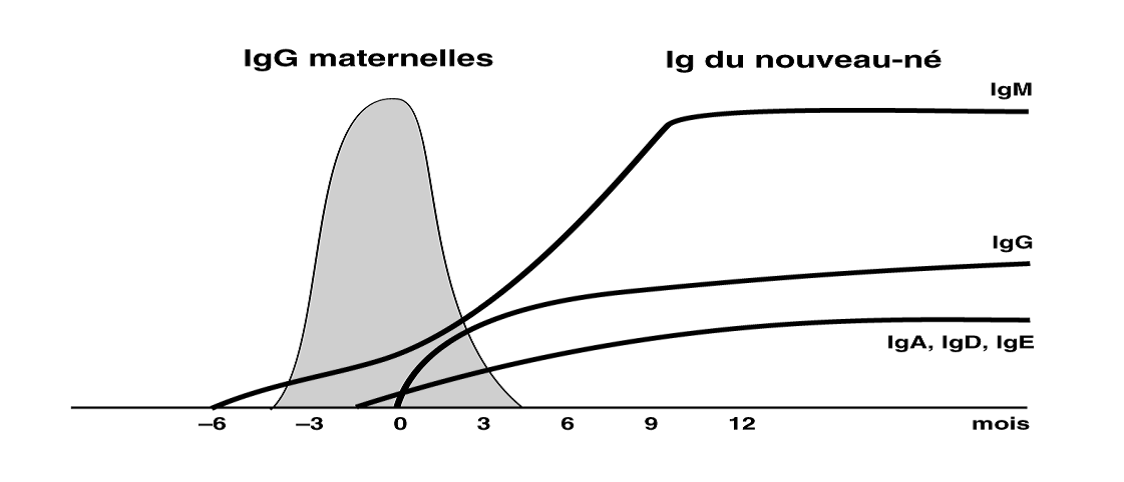
Source : Jean-Pierre REGNAULT, Immunologie générale.
Adolescents
En général, cette période d’âge est celle où le système immunitaire répond le mieux.
Personnes âgées
La capacité d’obtenir une bonne réponse immunitaire s’atténue au cours du vieillissement, car le pool des plasmocytes non différenciés diminue avec le temps.
Facteurs génétiques
Les déterminants génétiques, tels que le système sanguin ABO et les antigènes d’histocompatibilité HLA, jouent un rôle dans l’immunité adaptative.
Certaines personnes répondent mieux que d’autres aux vaccins. Par exemple, certaines personnes ne développent pas d’anticorps à la suite de la vaccination contre l’hépatite B, mais développent une réponse cellulaire qui assure leur protection.
Immunodépression
Qu’elle soit acquise ou congénitale, l’immunodépression diminue généralement la réponse immunitaire humorale ou la réponse immunitaire cellulaire, ou les deux.
Malnutrition
La malnutrition est associée à une altération de la fonction de la barrière intestinale et à un faible niveau des protéines du complément.
Le tissu lymphatique, en particulier le thymus, subit une atrophie, et les réponses d'hypersensibilité de type retardé sont réduites.
Les niveaux d'anticorps produits après la vaccination sont réduits chez les personnes gravement malnutries.
Obésité
L’obésité est associée à des troubles métaboliques qui provoquent un dysfonctionnement tissulaire dans le tissu adipeux, le foie, le pancréas et les vaisseaux sanguins.
Ces changements sont associés à un impact négatif sur l’immunité contre l’infection et sur l’efficacité vaccinale.
DerniÃĻre mise à jour : 16 avril 2021
